Содержание
Из Википедии — свободной энциклопедии
Реакция серебряного зеркала — это реакция восстановления серебра из аммиачного раствора оксида серебра (реактив Толленса). В водном растворе аммиака оксид серебра растворяется с образованием комплексного соединения — гидроксид диамминсеребра(I) [Ag(NH3)2]OH
A g 2 O + 4 N H 3 ⋅ H 2 O ⇄ 2 O H + 3 H 2 O O+4NH_\cdot H_O\rightleftarrows 2OH+3H_O>>>
при добавлении к которому альдегида происходит окислительно-восстановительная реакция с образованием металлического серебра:
RCHO + 2 O H → τ o C 2 A g ↓ + RCOONH 4 + 3 N H 3 + H 2 O >+2OH\ C>>\ 2Ag\downarrow +>_+3NH_+H_O>>>
Если реакция проводится в сосуде с чистыми и гладкими стенками, то серебро осаждается на них в виде тонкой плёнки, образуя зеркальную поверхность. При наличии малейших загрязнений серебро выделяется в виде серого рыхлого осадка.
Реакция «серебряного зеркала» может использоваться как качественная реакция на альдегиды. Так, реакцию «серебряного зеркала» можно использовать как отличительную между глюкозой и фруктозой. Глюкоза относится к альдозам (содержит альдегидную группу в открытой форме), а фруктоза — к кетозам (содержащие кетогруппу в закрытой форме). Поэтому глюкоза дает реакцию «серебряного зеркала», а фруктоза — нет. Но если в растворе присутствует щелочная среда, то кетозы изомеризуются в альдозы и также дают положительные пробы Фелинга.
Источник
Целлюлоза (клетчатка)
Целлюлоза – наиболее распространенный растительный
полисахарид. Она обладает большой механической прочностью и исполняет роль
опорного материала растений. Древесина содержит 50-70% целлюлозы, хлопок
представляет собой почти чистую целлюлозу.
Как и у крахмала, структурной единицей целлюлозы
является D-
глюкопираноза, звенья которой связаны (1-4) -гликозидными связями. Однако, от
крахмала целлюлоза отличается b- конфигурацией гликозидных связей
между циклами и строго линейным строением.
Целлюлоза состоит из нитевидных молекул, которые
водородными связями гидроксильных групп внутри цепи, а также между соседними
цепями собраны в пучки. Именно такая упаковка цепей обеспечивает высокую
механическую прочность, волокнистость, нерастворимость в воде и химическую
инертность, что делает целлюлозу идеальным материалом для построения клеточных
стенок.
b- Гликозидная связь не разрушается пищеварительными ферментами человека,
поэтому целлюлоза не может служить ему пищей, хотя в определенном количестве
является необходимым для нормального питания балластным веществом. В желудках
жвачных животных имеются ферменты, расщепляющие целлюлозу, поэтому такие
животные используют клетчатку в качестве компонента пищи.
Несмотря на нерастворимость целлюлозы в воде и обычных
органических растворителях, она растворима в реактиве Швейцера (раствор
гидроксида меди в аммиаке), а также в концентрированном растворе хлористого
цинка и в концентрированной серной кислоте.
Как и крахмал, целлюлоза при кислотном гидролизе дает
глюкозу.
Целлюлоза – многоатомный спирт, на элементную ячейку
полимера приходятся три гидроксильных группы. В связи с этим, для целлюлозы
характерны реакции этерификации (образование сложных эфиров). Наибольшее
практическое значение имеют реакции с азотной кислотой и уксусным ангидридом.
|
целлюлоза |
+ 3n HNO3 |
H2SO4 –––– |
тринитрат целлюлозы |
+ 3nH2О |
Полностью
этерифицированная клетчатка известна под названием пироксилин, который после
соответствующей обработки превращается в бездымный порох. В зависимости от
условий нитрования можно получить динитрат целлюлозы, который в технике
называется коллоксилином. Он так же используется при изготовлении пороха и
твердых ракетных топлив. Кроме того, на основе коллоксилина изготавливают
целлулоид.
При взаимодействии целлюлозы с уксусным ангидридом в
присутствии уксусной и серной кислот образуется триацетилцеллюлоза.
|
+ 3n |
триацетилцеллюлоза |
+ 3n СH3СOOН |
Триацетилцеллюлоза (или ацетилцеллюлоза) является ценным продуктом для
изготовления негорючей кинопленки и ацетатного шелка. Для этого ацетилцеллюлозу
растворяют в смеси дихлорметана и этанола и этот раствор продавливают через
фильеры в поток теплого воздуха. Растворитель испаряется и струйки раствора
превращаются в тончайшие нити ацетатного шелка.
Целлюлоза не дает реакции «серебряного зеркала».
Говоря о применении целлюлозы, нельзя не сказать о том, что большое
количество целлюлозы расходуется для изготовления различной бумаги. Бумага –
это тонкий слой волокон клетчатки, проклеенный и спрессованный на специальной
бумагоделательной машине.
Из приведенного выше уже видно, что использование
целлюлозы человеком столь широко и разнообразно, что применению продуктов
химической переработки целлюлозы можно посвятить самостоятельный раздел.
Химические свойства глюкозы
Водный раствор глюкозы
В водном растворе глюкозы существует динамическое равновесие между двумя циклическими формами — α и β и линейной формой:
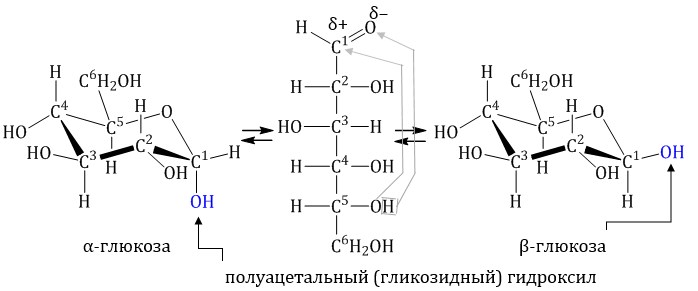
Реакции на карбонильную группу — CH=O
Глюкоза проявляет свойства, характерные для альдегидов.
Реакция «серебряного зеркала»
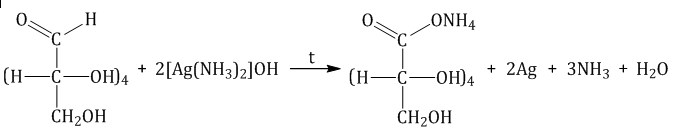
Реакция с гидроксидом меди (II) при нагревании. При взаимодействии глюкозы с гидроксидом меди (II) выпадает красно-кирпичный осадок оксида меди (I):
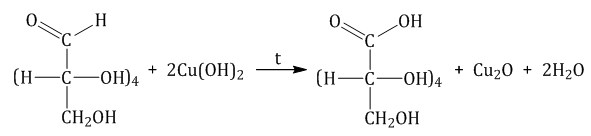
Окисление бромной водой. При окислении глюкозы бромной водой образуется глюконовая кислота:
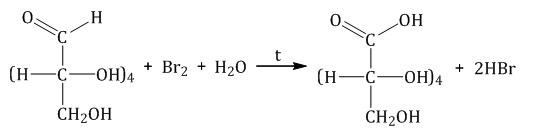
Также глюкозу можно окислить хлором, бертолетовой солью, азотной кислотой.
| Концентрированная азотная кислота окисляет не только альдегидную группу, но и гидроксогруппу на другом конце углеродной цепи. |
Каталитическое гидрирование. При взаимодействии глюкозы с водородом происходит восстановление карбонильной группы до спиртового гидроксила, образуется шестиатомный спирт – сорбит:
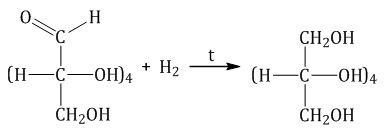
Брожение глюкозы. Брожение — это биохимический процесс, основанный на окислительно-восстановительных превращениях органических соединений в анаэробных условиях.
Спиртовое брожение. При спиртовом брожении глюкозы образуются спирт и углекислый газ:
C6H12O6 → 2C2H5OH + 2CO2
Молочнокислое брожение. При молочнокислом брожении глюкозы образуется молочная кислота:
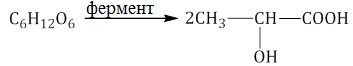
Маслянокислое брожение. При маслянокислом брожении глюкозы образуется масляная кислота (внезапно):
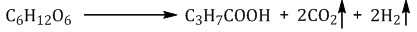
Образование эфиров глюкозы (характерно для циклической формы глюкозы).
Глюкоза способна образовывать простые и сложные эфиры.
Наиболее легко происходит замещение полуацетального (гликозидного) гидроксила.
Например, α-D-глюкоза взаимодействует с метанолом.
При этом образуется монометиловый эфир глюкозы (α-O-метил-D-глюкозид):
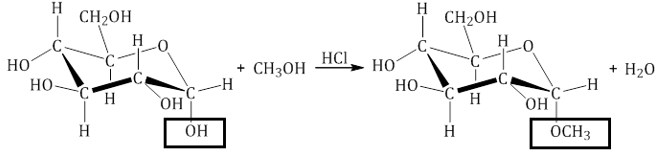
| Простые эфиры глюкозы получили название гликозидов. |
В более жестких условиях (например, с CH3-I) возможно алкилирование и по другим оставшимся гидроксильным группам.
Моносахариды способны образовывать сложные эфиры как с минеральными, так и с карбоновыми кислотами.
| Например, β-D-глюкоза реагирует с уксусным ангидридом в соотношении 1:5 с образованием пентаацетата глюкозы (β-пентаацетил-D-глюкозы): |
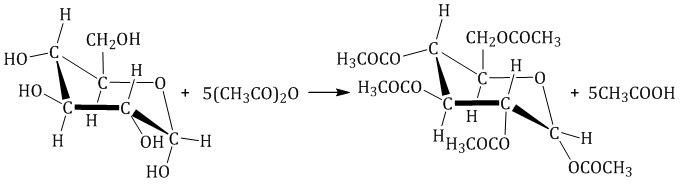
Активность в солях, благородство в чистоте
Серебро — металл довольно-таки стойкий, в воде не ржавеет и не растворяется. Можно посеребрить воду, но никто не скажет, что это раствор серебра. Вода останется водой, пусть даже облагороженной и продезинфицированной. Так очищать воду научились в давние времена и до сих пор используют этот способ в фильтрах.
Зато соли и оксиды серебра охотно вступают в химические реакции и растворяются в жидкостях, в результате чего возникают новые вещества, которые оказываются востребованными как в технике, так и в быту.
Формула простая — Ag2O. Два атома серебра и атом кислорода образуют оксид серебра, обладающий чувствительностью к свету. Однако в фотографии большее применение нашли другие соединения, зато оксид проявил расположенность к реактивам аммиака. В частности к нашатырному спирту, который еще наши бабушки использовали, чтобы очистить изделия, когда они потемнели.
Аммиак — соединение азота и водорода (NH3). Азот составляет 78% земной атмосферы. Он повсюду, как один из самых распространенных элементов на Земле. Водно-аммиачный раствор настолько широко применяется, что получил сразу несколько названий: аммиачная вода, едкий аммоний, гидроксид аммония, едкий аммиак. Легко запутаться в таком ряду синонимов. Если развести аммиачную воду до слабого, 10%-ного раствора, получим нашатырный спирт.
Когда химики растворили оксид в аммиачной воде, миру явилось новое вещество — комплексное соединение гидроксид диамин серебра с весьма привлекательными свойствами.
Процесс описывается химической формулой: Ag2O + 4NH4OH = 2OH + 3H2O.

Процесс и формула химической реакции аммиачной воды и оксида серебра
Применение глюкозы:
Глюкоза используется в различных отраслях промышленности и быту:
– в медицине в качестве лечебного средства, для приготовления лечебных препаратов и пр.;
– в пищевой промышленности при выпечке хлеба, а также при производстве сгущённого молока и мороженого, в кондитерском деле при изготовлении мармелада, карамели, пряников и т.д.;
– в сельском хозяйстве в пчеловодстве для подкормки пчёл;
– в текстильной промышленности при крашении и печатании рисунков;
– в химической промышленности в качестве исходного продукта при производстве аскорбиновых и глюконовых кислот, для синтеза ряда производных сахаров и т.д.;
– в производстве зеркал и елочных игрушек (серебрение);
– в микробиологической промышленности как питательная среда для получения кормовых дрожжей;
– в приготовлении пищи и кормов для животных используются процессы молочнокислого, спиртового и маслянокислого брожения.
Примечание: Фото https://www.pexels.com, https://pixabay.com.
Найти что-нибудь еще?
карта сайта
Коэффициент востребованности
3 878
Искусственно состаренные серебряные отражающие поверхности
Мода на антикварные предметы интерьера никогда не проходит, и не обошла она даже зеркала. Но не всем удается приобрести именно то зеркало, которое несколько десятков лет назад украшало какой-нибудь театр или зажиточный дом. Поэтому некоторые производители прибегают к разнообразным технологиям и средствам, позволяющим визуально состарить отражающие стекла. Это достигается не только внешним изменением зеркальной рамки с помощью потертости или обесцвечивания. Все дело заключается в искусственном воздействии на амальгаму. В искусственно состаренных зеркалах она специально сделана темной, тусклой, с черными патинированными вкраплениями. Такие зеркала часто имеют не только тусклую серебряную амальгаму, но в них также присутствуют разноцветные зеркальные полотна (оттенки их могут быть самыми разными). Благодаря данным процессам изображения в отражении получаются насыщенными и яркими. В некоторых состаренных стеклах изображение порой получается трехмерным, но при этом отражение нисколько не искажается.
Данный антиквариат становится очень популярным среди любителей старинных вещей. И если физическое воздействие может отрицательно повлиять на качество отражения, то воздействие на химическом уровне никак не повлияет на зеркальные характеристики и их способность выполнять свои прямые функции. Помимо этого, на поверхность искусственно состаренных зеркал наносится слоистая смола. Такой предмет интерьера прослужит вам очень долго. Если вы не хотите смотреться в слишком старое зеркало, то можно заказать такой предмет, на котором лишь в некоторых частях стекла будет исправлена серебряная амальгама, например, в верхней части поверхности или только в уголках. Цветовая гамма состаренного стекла может быть самой разнообразной. Наиболее популярной среди любительниц покрутиться перед зеркалом является зеркальная поверхность с нежно-розовыми пятнами. Иногда используются плавно переходящие друг в друга оранжевые, фиолетовые и золотистые цвета.
Традиционное бесцветное серебряное зеркало
Традиционные зеркала изготавливаются по двум технологиям. Первая, которая уже не так распространена, как раньше, основана на изготовлении зеркал с добавлением алюминия. Их стоимость не так велика, но даже это не привлекает большое количество покупателей. Качество зеркал с добавлением алюминия оставляет желать лучшего. Именно поэтому их производство с каждым разом все больше и больше сокращается. На сегодняшний день все чаще можно встретить в магазинах бесцветные, с серебром. Они не только не боятся влаги, но и отличаются очень долгим сроком эксплуатации. Отражения в таком качественном стекле получаются глубокими, без искажений. Данные зеркала изготавливаются на серебряной амальгаме. Процесс ее изготовления включает накаливание серебра и смешивание его с ртутью. Другой вариант – добавление в раскаленную ртуть серебряного порошка. Данные ингредиенты хорошенько перемешиваются в тигле железной лопаткой, затем ее промывают и пропускают через замшевый материал. Как становится понятно из описания, изготовить серебряную амальгаму можно и самостоятельно.
Но этот процесс может быть достаточно опасным, если вы не воспользуетесь средствами защиты органов дыхания (ртуть – очень летучий металл, а при нагревании выделяет смертельно опасные пары). Поэтому, если у вас нет особого оборудования для этого, не стоит рисковать и лучше приобрести зеркало в магазине. На сегодняшний день процесс изготовления серебряной зеркальной поверхности включает в себя нанесение на стекло нескольких защитных слоев. Итак, первым из них является слой серебряной амальгамы. Затем ее покрывают серебряным фильмом. Готовую зеркальную поверхность обрабатывают медным слоем, который позволяет защитить предыдущие слои от проникновения в них влаги. Третьим слоем является полимерное покрытие.
Химические свойства глюкозы
Химические свойства глюкозы, как и других альдоз, обусловлены присутствием в ее молекуле: а)альдегидной группы; б) спиртовых гидроксилов; в) полуацетального (гликозидного) гидроксила.
Специфические свойства
1. Брожение (ферментация) моносахаридов
Важнейшим свойством моносахаридов является их ферментативное брожение, т.е. распад молекул на осколки под действием различных ферментов. Брожению подвергаются в основном гексозы в присутствии ферментов, выделяемых дрожжевыми грибками, бактериями или плесневыми грибками. В зависимости от природы действующего фермента различают реакции следующих видов:
1) Спиртовое брожение
2) Молочнокислое брожение
(образуется в организмах высших животных при мышечных сокращениях).
3) Маслянокислое брожение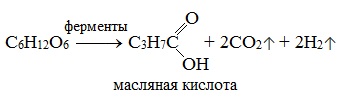
4) Лимоннокислое брожение
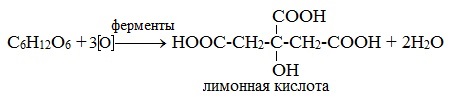
Реакции с участием альдегидной группы глюкозы (свойства глюкозы как альдегида)
1. Восстановление (гидрирование) с образованием многоатомного спирта
В ходе этой реакции карбонильная группа восстанавливается и образуется новая спиртовая группа:
Cорбит содержится во многих ягодах и фруктах, особенно много сорбита в плодах рябины.
2. Окисление
1) Окисление бромной водой
Качественные реакции на глюкозу как альдегид!
Протекающие в щелочной среде при нагревании реакции с аммиачным раствором Ag2O (реакция серебряного зеркала») и с гидроксидом меди (II) Cu (OH)2 приводят к образованию смеси продуктов окисления глюкозы.
2) Реакция серебряного зеркала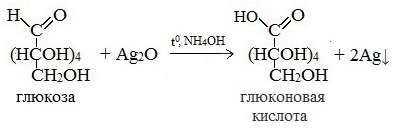
Соль этой кислоты – глюконат кальция – известное лекарственное средство.
Видеоопыт «Качественная реакция глюкозы с аммиачным раствором оксида серебра (I)»
3) Окисление гидроксидом меди (II)
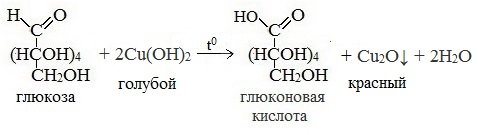
В ходе этих реакций альдегидная группа – СНО окисляется до карбоксильной группы – СООН.
Реакции глюкозы с участием гидроксильных групп (свойства глюкозы как многоатомного спирта)
1. Взаимодействие с Cu (ОН)2с образованием глюконата меди (II)
Качественная реакция на глюкозу как многоатомный спирт!
Подобно этиленгликолю и глицерину, глюкоза способна растворять гидроксид меди (II), образуя растворимое комплексное соединение синего цвета:
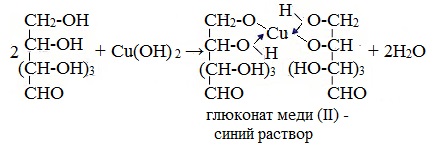
Прильём к раствору глюкозы несколько капель раствора сульфата меди (II) и раствор щелочи. Осадка гидроксида меди не образуется. Раствор окрашивается в ярко-синий цвет.
В данном случае глюкоза растворяет гидроксид меди (II) и ведет себя как многоатомный спирт, образуя комплексное соединение.
Видеоопыт «Качественная реакция глюкозы с гидроксидом меди (II)»
2. Взаимодействие с галогеналканами с образованием простых эфиров
Являясь многоатомным спиртом, глюкоза образует простые эфиры:
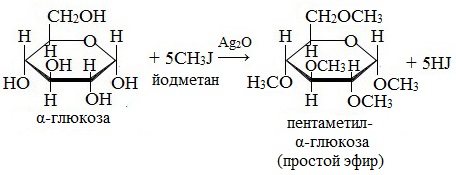
Реакция происходит в присутствии Ag2O для связывания выделяющегося при реакции НI.
3. Взаимодействие с карбоновыми кислотами или их ангидридами с образованием сложных эфиров.
Например, с ангидридом уксусной кислоты: 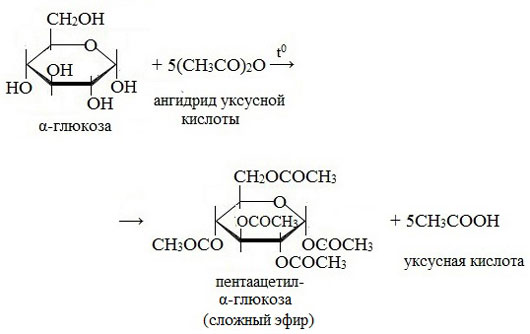
Реакции с участием полуацетального гидроксила
1. Взаимодействие со спиртами с образованием гликозидов
Гликозиды – это производные углеводов, у которых гликозидный гидроксил замещен на остаток какого-либо органического соединения.
Содержащийся в циклических формах глюкозы полуацетальный (гликозидный) гидроксил является очень реакционноспособным и легко замещается на остатки различных органических соединений.
В случае глюкозы гликозиды называются глюкозидами. Связь между углеводным остатком и остатком другого компонента называется гликозидной.
Гликозиды построены по типу простых эфиров.
При действии метилового спирта в присутствии газообразного хлористого водорода атом водорода гликозидного гидроксила замещается на метильную группу:
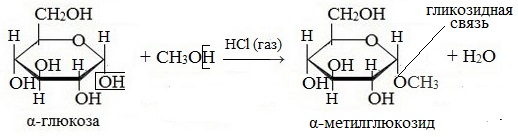
В данных условиях в реакцию вступает только гликозидный гидроксил, спиртовые гидроксильные группы в реакции не участвуют.
Гликозиды играют чрезвычайно важную роль в растительном и животном мире. Существует огромное число природных гликозидов, в молекулах которых с атомом С (1) глюкозы остатки самых различных соединений.
Реакции окисления
Более сильный окислитель – азотная кислота НNO3 – окисляет глюкозу до двухосновной глюкаровой (сахарной) кислоты:
В ходе этой реакции и альдегидная группа – СНО и первичная спиртовая группа — СН2ОН окисляются до карбоксильных – СООН.
Видеоопыт Окисление глюкозы кислородом воздуха в присутствии метеленового голубого
Рубрики: Углеводы Теги: Углеводы
Углеводы. Генетический D- ряд сахаров
«Углеводы широко распространены в природе и выполняют в живых
организмах различные важные функции. Они поставляют энергию для биологических
процессов, а также являются исходным материалом для синтеза в организме других
промежуточных или конечных метаболитов. Углеводы имеют общую формулу Cn(H2O)m, откуда и возникло название
этих природных соединений.
Углеводы делятся на простые сахара или моносахариды и полимеры этих
простых сахаров или полисахариды. Среди полисахаридов следует выделить группу
олигосахаридов, содержащих в молекуле от 2 до 10 моносахаридных остатков. К ним
относятся, в частности, дисахариды.
Моносахариды являются гетерофункциональными соединениями. В их молекулах
одновременно содержатся и карбонильная (альдегидная или кетонная), и несколько
гидроксильных групп, т.е. моносахариды представляют собой
полигидроксикарбонильные соединения — полигидроксиальдегиды и
полигидроксикетоны. В зависимости от этого моносахариды подразделяются на
альдозы (в моносахариде содержится альдегидная группа) и кетозы (содержится
кетогруппа). Например, глюкоза – это альдоза, а
фруктоза – это кетоза.
(глюкоза
(альдоза)) (фруктоза (кетоза))
В зависимости от числа атомов углерода в молекуле
моносахарид называется тетрозой, пентозой, гексозой и т.д. Если объединить
последние два типа классификации, то глюкоза – это альдогексоза, а фруктоза –
кетогексоза. Большинство встречающихся в природе моносахаридов – это пентозы и
гексозы.
Моносахариды изображаются в виде проекционных формул
Фишера, т.е. в виде проекции тетраэдрической модели атомов углерода на
плоскость чертежа. Углеродная цепь в них записывается вертикально. У альдоз
наверху помещают альдегидную группу, у кетоз – соседнюю с карбонильной
первичноспиртовую группу. Атом водорода и гидроксильную группу при
асимметрическом атоме углерода располагают на горизонтальной прямой.
Асимметрический атом углерода находится в образующемся перекрестье двух прямых
и не обозначается символом. С групп, расположенных вверху, начинают нумерацию
углеродной цепи. (Дадим определение асимметрическому атому углерода: это атом
углерода, связанный с четырьмя различными атомами или группами).
Установление абсолютной конфигурации, т.е. истинного
расположения в пространстве заместителей у асимметрического атома углерода
является весьма трудоемкой, а до некоторого времени было даже невыполнимой
задачей. Существует возможность характеризовать соединения путем сравнения их конфигураций
с конфигурациями эталонных соединений, т.е. определять относительные
конфигурации.
Относительная конфигурация моносахаридов определяется по
конфигурационному стандарту – глицериновому альдегиду, которому еще в конце
прошлого столетия произвольно были приписаны определенные конфигурации,
обозначенные как D- и L- глицериновые
альдегиды. С конфигурацией их асимметрических атомов углерода сравнивается
конфигурация наиболее удаленного от карбонильной группы асимметрического атома
углерода моносахарида. В пентозах таким атомом является четвертый атом углерода
(С4), в гексозах – пятый (С5), т.е.
предпоследние в цепи углеродных атомов. При совпадении конфигурации этих атомов
углерода с конфигурацией D-
глицеринового альдегида моносахарид относят к D- ряду. И, наоборот, при совпадении с конфигурацией L- глицеринового
альдегида считают, что моносахарид принадлежит к L- ряду. Символ D означает, что
гидроксильная группа при соответствующем асимметрическом атоме углерода в
проекции Фишера располагается справа от вертикальной линии, а символ L- что
гидроксильная группа расположена слева.
Опыт 4. Окисление глюкозы аммиачным раствором оксида серебра (реакция «серебряного зеркала»)
Реактивы и материалы: глюкоза, 0,5%-ный раствор; нитрат серебра, 0,2 н. раствор; аммиак, 2 н. раствор; едкий натр, 2 н. раствор.
В пробирку помещают каплю раствора нитрата серебра, 2 капли раствора едкого натра и приливают по каплям раствор аммиака до растворения образовавшегося осадка гидроксида серебра. Затем добавляют 1 каплю раствора глюкозы и слегка подогревают содержимое пробирки над пламенем горелки до начала почернения раствора. Дальше реакция идет без нагревания, и металлическое серебро выделяется на стенках пробирки в виде блестящего зеркального налета. Химизм процесса:
Моносахариды легко окисляются, причем в зависимости от условий получаются разнообразные продукты окисления
При осторожном окислении альдоз в кислой или нейтральной среде образуются альдоновые кислоты(одноосновные многоатомные оксикислоты). Кетозы (например, фруктоза) в этих условиях не окисляются
При окислении моносахаридов в щелочной среде происходит их глубокое расщепление с образованием ряда продуктов, в том числе очень легко окисляющихся. Поэтому моносахариды являются сильными восстановителями.
При окислении моносахаридов в щелочном растворе не удается выделить продукты окисления с тем же числом углеродных атомов (как альдоновые кислоты при окисления альцоз в кислой среде).
Подобно альдегидам, моносахариды восстанавливают аммиачный раствор оксида серебра с образованием осадка металлического серебра («серебряного зеркала»). Эту реакцию дают как альдозы, так и кетозы.
Окисление оксидом серебра в щелочной среде служит качественной реакцией на моносахариды.
Примечание. Пробирку для опыта необходимо тщательно вымыть (обезжирить) — прокипятить со щелочью и промыть водой. Если стенки пробирки грязные, то металлическое серебро выделяется в виде черного осадка.
Источник
Получение сахарозы из сахарного тростника:
Сахарный тростник является основной мировой культурой для производства сахара. На его долю приходится до 65 % мирового производства сахара.
Сахарный тростник до начала цветения срезают. Срезанные стебли измельчают и размалывают. Из полученной массы отжимают сок, в котором содержится до 0,03 % белковых веществ, 0,1 % зернистых веществ (крахмала), 0,22 % азотосодержащей слизи, 0,29 % солей (большей частью органических кислот), 18,36 % сахара, 81 % воды и очень небольшое количество ароматических веществ, придающих сырому соку своеобразный запах.
Для очистки сока к нему добавляют свежегашеную известь – Са(ОН)2 и нагревают. Сахароза вступает в химическую реакцию с гидроксидом кальция, в результате чего образуется растворимый в воде сахарат кальция. Кроме того, другие вещества, содержащиеся в соке, также вступают в реакцию с гидроксидом кальция, образуя малорастворимые и нерастворимые соли, которые выпадают в осадок и отфильтровывают.
Затем через раствор, чтобы разложить сахарат кальция и нейтрализовать избыточный гидроксид кальция, пропускают углекислый газ – СО2. В итоге образуется карбонат кальция – СаСО3, который выпадает в осадок. Выпавший в осадок карбонат кальция отфильтровывают, а раствор выпаривают в вакуумных аппаратах до получения кристаллов сахарозы. На данной стадии производства сахароза все еще содержит примеси – мелассу и имеет коричневый цвет. Меласса придает сахарозе ярко выраженный естественный аромат и вкус. Полученный продукт именуется коричневым сахаром или тростниковым нерафинированным сахаром. Он (коричневый сахар) пригоден в пищу. Его можно использовать в пищу как есть либо подвергнуть дополнительной очистке.
На последней стадии производства сахарозу подвергают дополнительной очистке и обесцвечиванию. В конечном итоге получают рафинированный (очищенный) сахар, имеющий белый цвет.
Получение и производство глюкозы:
В природе глюкоза образуется в результате реакции фотосинтеза и содержится в различных частях растений: листьях и плодах. У животных глюкоза образуется в результате расщепления гликогена.
Глюкоза образуется в ходе следующих химических реакций:
1. реакции сахарозы с водой (гидролиз сахарозы):
С12Н22О11 + Н2О → С6Н12O6 + С6Н12O6 (tо, kat = H2SO4, HCl).
При гидролизе (при нагревании в присутствии ионов водорода) сахароза расщепляется на составляющие ее моносахариды – глюкозу и фруктозу за счёт разрыва гликозидных связей между ними. Данная реакция является обратной процессу образования сахарозы из моносахаридов.
Аналогичная реакция происходит в кишечнике у живых организмов при попадании в него сахарозы. В кишечнике сахароза под действием ферментов быстро гидролизуется на глюкозу и фруктозу.
2. реакции мальтозы с водой (гидролиз мальтозы):
С12Н22О11 + Н2О → 2С6Н12O6 (tо, kat = H2SO4, HCl).
При гидролизе (при нагревании в присутствии ионов водорода) мальтоза расщепляется на составляющие ее моносахариды – две молекулы глюкозы за счёт разрыва гликозидных связей между ними. Данная реакция является обратной процессу образования мальтозы из моносахаридов.
Аналогичная реакция происходит в кишечнике у живых организмов при попадании в него мальтозы. В кишечнике сахароза под действием ферментов быстро гидролизуется на две молекулы глюкозы.
3. реакции крахмала с водой (гидролиз крахмала):
(C6H10O5)n + nН2О → nС6Н12O6 (tо, kat = H2SO4).
Важнейшее свойство крахмала – способность подвергаться гидролизу под действием ферментов или при нагревании с кислотами.
Гидролиз протекает ступенчато. Из крахмала сначала образуется декстрин ((C6H10O5)n), который гидролизуется до мальтозы (C12H22O11). Затем в результате гидролиза мальтозы образуется глюкоза (С6Н12O6).
Аналогичная реакция происходит во рту, желудке и кишечнике у живых организмов при попадании в него крахмала. В желудке и кишечнике крахмал под действием ферментов окончательно гидролизуется на глюкозу.
Данная реакция используется в качестве промышленного способа получения глюкозы.
4. реакции А.М. Бутлерова – альдольной конденсации формальдегида:
CH2O → С6Н12O6 (kat = Ca(OH)2).
Первый синтез углеводов из формальдегида в щелочной среде осуществил А.М. Бутлеров в 1861 году.
Формальдегид под действием гидроксидов щелочноземельных металлов вступает в реакцию самоконденсации, образуя при этом смесь углеводов («формозу»), в т.ч. глюкозу.
5. реакции фотосинтеза:
CO2 + H2O → С6Н12O6 + O2 (hv, kat = хлорофилл).
В природе глюкоза образуется в растениях в результате фотосинтеза из углекислого газа и воды под действием солнечного света в листьях растений. В ходе реакции помимо глюкозы образуется кислород.
6. реакции гидролиза гликогена в кислой среде:
(C6H10O5)n → (C6H10O5)y → C6H12O6 (H2O, Н+).
Важнейшее свойство гликогена – способность подвергаться гидролизу в водных растворах кислот.
Гидролиз протекает ступенчато. Из гликогена ((C6H10O5)n) сначала образуется декстрин ((C6H10O5)y, при этом y < n), который гидролизуется до глюкозы (С6Н12O6).
Как провести реакцию в домашних условиях
Для того чтобы провести восстановление серебра из его оксида не в лабораторных условиях, необходимо в воде растворить азотнокислое серебро. Взять его можно в аптеке. Это ляписный карандаш. Воду лучше использовать дистиллированную. Получить ее можно простой конденсацией воды, испаряющейся из кипящего чайника. Если исходить из полулитровой емкости, то в таком количестве раствора азотнокислого серебра необходимо растворить еще нашатырный спирт (1 ч. л.). Сюда же нужно добавить 2-3 капли формальдегида — формалина.
Все реактивы вступают в реакцию не сразу, поэтому взболтайте как следует раствор и оставьте его в покое примерно на сутки. Если все пройдет успешно, то за этот срок ваша банка покроется тонким металлическим слоем. Таким же слоем покроется тот предмет, который вы поместите в банку.
Реакция серебро зеркало формула
3556 дн. с момента как существует сайт
Владельцы сайта
Реакция серебряного зеркала
«Химиком никоим образом стать невозможно,
и не принимаясь за химические операции»
Незадолго до урока была обнаружена древняя рукопись, предназначенная учащимся 10-го класса. Давайте её прочтём.

Дозвольте поведать вам о государстве нашем, ежели оно вам по сердцу.
Государство наше таково, что формулы веществ наших состоят только из трёх элементов.
И главным является Карбонил.
А теперь аз есмь желаю знати: ведаете ли вы, как именуется оно?
Огласите и запишите ваши ответы.
К сему руку приложил Формалин.
Вы можете представить себе жизнь без зеркал?
Ежели бы вы проснулись утром — и не увидели своего милого лика?
Недаром сказочных персонажей в качестве наказания лишали отражения.
Сегодня мы поговорим о зеркалах.

Огласите и запишите ваши ответы.
2. Для начала мы обратимся к словарям и выясним, что же такое зеркало.
Источник